Augen auf bei Nachfolgeartikeln
Hinweis
Es handelt sich bei dem Inhalt dieser Seite um eine frühere Veröffentlichung. Bitte beachten Sie, dass die Aussagen gegebenenfalls nicht mehr der aktuellen Rechts- und Vertragslage entsprechen.
Bei Fragen hilft Ihnen das DAP-Team auch gerne persönlich weiter – schreiben Sie einfach eine E-Mail an insonderfo@anderesdeutschesapothekenportal.de.
Nimmt ein Hersteller sein Arzneimittel vom Markt, wird es in der Datenbank mit AV (außer Vertrieb) gekennzeichnet. Bei AV-Artikeln wird in manchen Fällen ein Nachfolgeartikel vom Hersteller angeboten, der, falls er über die IFA und die ABDATA an den Apothekensoftwareanbieter weitergeleitet wurde, direkt mit dem Vorgängerartikel verknüpft wird. Das Vorhandensein eines Nachfolgeartikels wird also direkt beim Aufruf des AV-Artikels durch ein „N“ hinter der AV-Kennzeichnung sichtbar.
Durch Klicken auf das „N“ wird in den meisten Softwaresystemen die Nachfolge-PZN angezeigt. Oft öffnet sich im Kassendialog auch ein Fenster mit der Auswahlmöglichkeit, direkt den Nachfolgeartikel zu bestellen. An dieser Stelle ist allerdings Vorsicht geboten, denn ein AV-Artikel kann nicht in jedem Fall durch seinen Nachfolgeartikel ersetzt werden.
Dies kann verschiedene Gründe haben:
Nicht jeder Nachfolgeartikel ist aut-idem-konform zu seinem Vorgängerartikel.
Gemäß § 9 Rahmenvertrag muss das für die Abgabe ausgewählte Fertigarzneimittel (Nachfolgeartikel) gegenüber dem ärztlich verordneten Fertigarzneimittel (Vorgängerartikel) folgende Kriterien erfüllen:
- Gleicher Wirkstoff
- Identische Wirkstärke
- Identische Packungsgröße im Sinne des § 8
- Gleiche oder austauschbare Darreichungsform
- Zulassung für ein gleiches Anwendungsgebiet
Außerdem darf kein Verstoß gegen betäubungsmittelrechtliche Vorschriften vorliegen.
Nicht identische Packungsgröße
So hat zum Beispiel der Nachfolgeartikel zu Atorimib 10/10 100 St. N3 PZN 15387217 eine nicht identische Packungsgröße im Sinne des § 8 Rahmenvertrag. Der Nachfolgeartikel mit der PZN 17970932 trägt mit 90 Tabletten gar kein Normkennzeichen und ist daher nicht aut-idem-konform zu seinem Vorgängerartikel.

Keine identische Wirkstärke
Der Nachfolgeartikel zu Skyrizi 75 mg Injektionslösung i. e. Fertigspritze 2 St. ILO PZN 15373617 (nicht mehr in der Taxe gelistet) hatte eine andere Wirkstärke. Es handelt sich beim Nachfolgeartikel um nur eine Spritze mit 150 mg Risankizumab. Dieser Nachfolgeartikel ist ebenfalls nicht aut-idem-konform zum Vorgänger.

Unterschiedliche Zuordnung in der Packungsgrößenverordnung
Ein weiteres Beispiel war der Nachfolgeartikel von Tianeurax, der zwar ein identisches Normkennzeichen trug, aber aufgrund der enthaltenen Tablettenanzahl einer anderen Gruppe in der Packungsgrößenverordnung zugeordnet werden musste.
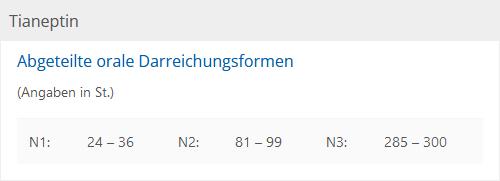
Ein Austausch ist auch hier nicht möglich, denn nach § 18 Abs. 1 Rahmenvertrag umfasst der Auswahlbereich bei Verordnungen, die eine N-Bezeichnung enthalten, nur den N-Bereich, der sich aus der Eingruppierung des verordneten Arzneimittels in die Anlage der PackungsV ergibt.
Nachfolgeartikel kein Rabattartikel
Ein weiteres Beispiel wäre das bei der AOK (z. B. Baden-Württemberg) rabattierte, aber AV gemeldete Atorvastatin AXiromed 80 mg Filmtabletten N3 PZN 13896245. Auch hier kann nicht ohne weiteres der Nachfolgeartikel mit der PZN 18303586 abgegeben werden, denn dieser ist nicht als rabattiert gemeldet. In diesem Fall müsste eines der vier preisgünstigsten Präparate vor dem nicht rabattierten Nachfolgeartikel abgegeben werden.
Es zeigt sich also anhand dieser Beispiele, dass auch wenn der Kassendialog die Bestellung eines Nachfolgeartikels anbietet, dies nicht immer die beste und vor allem nicht selten die falsche Entscheidung sein kann. Daher unser Rat: Augen auf bei Nachfolgeartikeln. Falls Sie sich unsicher sind, wenden Sie sich gerne mit Ihrer Frage an abgabeprobleme@extradeutschesapothekenportal.de.
Neuen Kommentar schreiben
Sie müssen angemeldet sein, um die Kommentarfunktion nutzen zu können.
Benutzeranmeldung
Geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden
DAP Newsletter
Immer aktuell informiert mit dem DAP Newsletter: zur Newsletter-Anmeldung
